一、电解原理
⑴.电解质溶液的导电
我们知道,金属导电时,是金属内部的自由电子发生的定向移动,而电解质溶液的导电与金属导电不同。
通电前电解质溶液中阴、阳离子在溶液中自由地移动;通电后在电场的作用下,这些自由移动的离子改作定向移动,带负电荷的阴离子由于静电作用向阳极移动,带正电荷的阳离子则向阴极移动。
电极名称:电解池中与直流电源负极相连的电极叫阴极,与直流电源正极相连的电极叫阳极。
物质能否导电是由其内部能否形成定向移动的自由电荷所决定的,对金属就是自由电子,而对电解质溶液就是自由移动的阴阳离子。
⑵.电解
①概念:使电流流过电解质溶液而在阴、阳两极引起氧化还原反应的过程叫电解。
②电子流动的方向:
电子从外接直流电源的负极流出,经导线到达电解池的阴极,电解池溶液中的阳离子移向阴极,并在阴极获得电子而被还原,发生还原反应;
与此同时,电解池溶液中的阴离子移向阳极,并在阳极上失去电子(也可能是阳极很活泼而本身失去电子)而被氧化,发生氧化反应。这样,电子又从电解池的阳极流出,沿导线而流回外接直流电源的正极。
③电极反应的类型:阳极反应为氧化反应,阴极反应为还原反应,故而阴极处于被保护的状态,而阳极则有可能被腐蚀。
(3)实验分析:电解CuCl2溶液
(1)电极材料
阴极可用惰性电极,甚至较活泼的金属,但阳极需使用惰性电极,否则会发生氧化反应而溶解。
(2)惰性电极一般指金、铂、石墨电极,银、铜等均是活性电极。
(3)实验现象:通电后,电流表指针发生偏转,阴极石墨棒上析出一层红色固体,阳极表面有气泡放出,可闻到刺激性气味。
(4)淀粉碘化钾试纸的作用:检验阳极产物是否为Cl2。使用时应先润湿并缠于玻棒端或用镊子夹持,作用时间不宜太久,否则变蓝后会被Cl2漂白。
(4)放电顺序
1)阳极上失电子的规律
应首先看电极材料是惰性电极,还是活性电极,如是惰性电极,则由溶液中的阴离子失去电子,阴离子的还原性越强越易失电子,阴离子的放电顺序为:S2->I->Br->Cl->OH->含氧酸根离子>F-;
电极材料是活性电极,则电极材料的金属先失去电子进入溶液,此时溶液中其他离子不再失电子。
(注:惰性电极材料:C、Pt、Au 活性电极材料:除C、Pt、Au外的其它金属)
2)阴极上得电子的规律
阴极上只能由溶液中阳离子获得电子,阳离子氧化性越强越易得电子,阳离子放电顺序一般为:
Ag+>Hg2+>Fe3+>Cu2+>H+(酸)>Fe2+>Zn2+>H+(水溶液)>Al3+>Mg2+>Na+>Ca2+>K+
3)变价的金属
Fe在作阳极发生氧化反应时电极反应为:Fe-2e-=Fe2+
(5)电解反应方程式的书写步骤:
①分析电解质溶液中存在的离子;
②分析离子的放电顺序;
③确定电极、写出电极反应式;
④写出电解方程式。如:
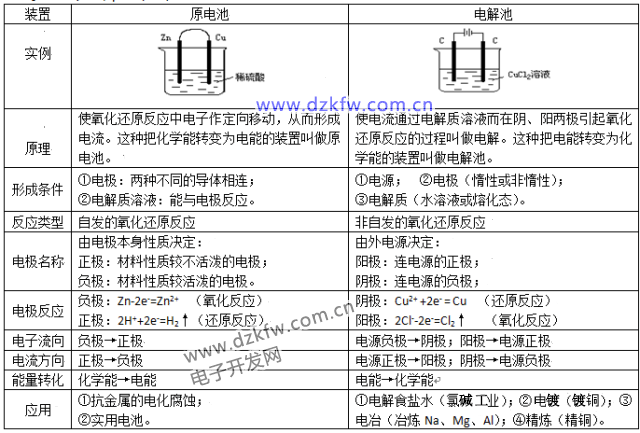
二、原电池和电解池的比较:
一.电解饱和食盐水反应原理
在U型管里装入饱和食盐水,滴入几滴酚酞试液,用碳棒作阳极、铁棒作阴极,将湿润的碘化钾淀粉试纸放在阳极附近,接通电源,观察管内发生的现象及试纸颜色的变化。
注意:铁棒不可作阳极,否则发生Fe-2e-=Fe2+;碘化钾淀粉试纸需事先用水润湿。
现象:阴、阳两极均有气体放出,阳极气体有刺激性气味,能使湿润的碘化钾淀粉试纸变蓝;阴极区域溶液变红。说明阴极区域生成物为碱性物质与H2,阳极产物是Cl2。
2.电解饱和食盐水反应原理
饱和食盐水成分:溶液存在Na+、Cl-、H+、OH-四种离子。
电极反应式:阴极:2H++2e-=H2↑(还原反应);
阳极:2Cl--2e-=Cl2↑(氧化反应)。
实验现象解释:
(1)阴极区域变红原因:由于H+被消耗,使得阴极区域OH-离子浓度增大(实际上是破坏了附近水的电离平衡,由于KW为定值,c(H+)因电极反应而降低,导致c(OH-)增大,使酚酞试液变红)。
(2)湿润的碘化钾淀粉试纸变蓝原因:氯气可以置换出碘化钾中的碘,Cl2+2KI=2KCl+I2,I2使淀粉变蓝。
注意:如果试纸被熏蒸的太久,蓝色会因为湿氯气的漂白作用而褪去。
电解饱和食盐水的总反应式:
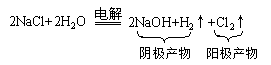
该电解反应属于放氢生碱型,电解质与水均参与电解反应,类似的还有K2S、MgBr2等。
二、铜的电解精炼
1.原理:电解时,用粗铜板作阳极,与直流电源的正极相连;用纯铜板作阴极,与电源的负极相连,用CuSO4溶液(加入一定量的硫酸)作电解液。
CuSO4溶液中主要有Cu2+、SO42-、H+、OH-,通电后H+和Cu2+移向阴极,并在阴极发生Cu2++2e-=Cu,OH-和SO42-移向阳极,但阳极因为是活性电极故而阴离子并不放电,主要为阳极(活泼及较活泼金属)发生氧化反应而溶解,阳极反应:Cu-2e-=Cu2+。
电解过程中,比铜活泼的Zn、Fe、Ni等金属杂质,在铜溶解的同时也会失电子形成金属阳离子而溶解,此时阴极仍发生Cu2++2e-=Cu,这会导致电解液浓度不发生变化;Ag、Au不如Cu易失电子,Cu溶解时它们以阳极泥沉积下来可供提炼Au、Ag等贵金属。
该过程实现了提纯铜的目的。
离子在电极上得失电子的能力与离子的性质、溶液的浓度、电流的大小、电极的材料等都有关系。中学阶段我们一般只讨论电极材料的性质、离子的氧化性强弱和还原性强弱对它们得失电子能力的影响
三、电解冶炼铝
工业上,用纯净的氧化铝为原料,采用电解的方法制取铝。
纯净的氧化铝熔点很高(2045℃),很难熔化,现在都用熔化的冰晶石(Na3AlF6)作熔剂,使氧化铝在1000℃左右溶解在液态的冰晶石里,成为冰晶石和氧化铝的熔融体,然后进行电解。
电极反应式:
阴极: 4Al3++12e-=4Al
阳极: 6O2-+12e-=3O2↑
总反应式:2Al2O3 ==4Al+3O2↑ (只能电解Al2O3,不能是AlCl3)
在冶炼铝时,阳极产生氧气,石墨阳极在如此高温条件下,将不断被氧气氧化而消耗,因而需不断补充石墨阳极。
四、电镀铜
1.原理:电镀时,一般都是用含镀层金属离子的电解质溶液为电镀液;把待镀金属制成品浸入电镀液中与直流电源的负极相连,作为阴极,而用镀层金属为阳极,阳极金属溶解在溶液中成为阳离子,移向阴极,并在阴极上被还原成金属析出。
电镀铜规律可概括为“阳极溶解,阴极沉积,电解液不变”。
工业上电镀常使用有毒电镀液,因此电镀废水应回收有用物质、降低有害物质含量后,达标排放,以防污染环境。
2.实验分析:电镀铜实验
(1)待镀件需酸洗去除表面的锈。
(2)电镀液CuSO4中加氨水制成铜氨溶液以降低Cu2+浓度使镀层光亮。
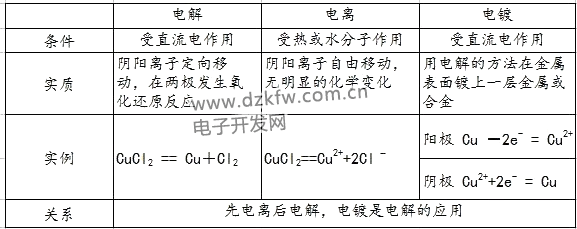
3.电解、电离和电镀的区别
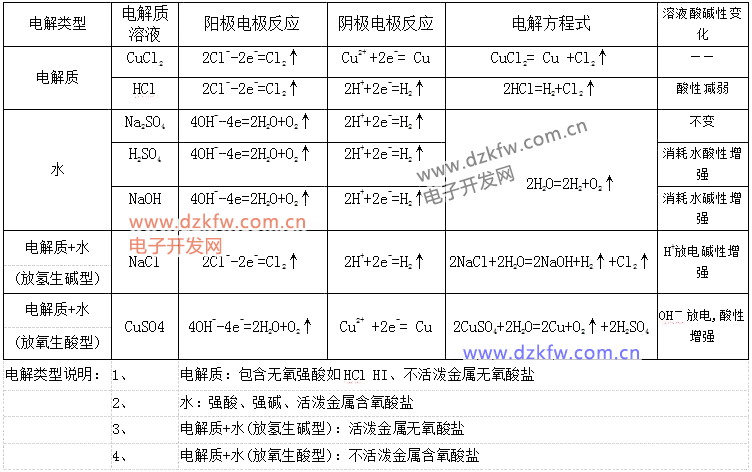
5.电解方程式的实例(用惰性电极电解):





 返回顶部
返回顶部 刷新页面
刷新页面 下到页底
下到页底